轮状病毒肠炎合并肠道外感染患儿免疫功能分析
2010-07-16周红胡岩韦国玉徐卫芹
周红 胡岩 韦国玉 徐卫芹
(江苏省沭阳县人民医院儿科 江苏沭阳 223600)
轮状病毒(rotavirus,RV)是秋、冬季小儿腹泻最常见的病原,人类感染轮状病毒后由于小肠上皮细胞黏膜受损导致细胞对体液和电解质控制能力丧失,肠道分泌与吸收能力失衡引起腹泻[1]。并引起全身多器官损害,如中枢神经系统、呼吸系统、循环血液系统、消化系统等损害[2]。其确切损伤机制尚不明确。本研究旨在了解轮状病毒肠炎合并肠道外感染患儿免疫功能变化,探讨免疫功能变化与RV发生肠道外感染的关系。
1 对象与方法
1.1 对象
选取于2008年10月至2009年2月间37例住院确诊为轮状病毒肠炎合并肠道外感染住院治疗的患儿为观察组,诊断标准依据《实用儿科学》第7版,大便轮状病毒检测(ELISA法)为阳性。其中男20例,女17例,平均年龄(32.3±6.57)个月;37例中合并呼吸道感染7例,心肌酶谱异常18例,肝功能异常12例。对照组20例为我院门诊体检的健康儿童,其中男11例,女9例,平均年龄(33.2±5.96)个月。近2周内无肠道感染,无过敏性及免疫相关的疾病。各组年龄、性别均无显著差异。
1.2 方法
T淋巴细胞亚群检测:花青藻红素-5(PE-CY5)标记抗CD3+抗体,异硫氰酸荧光素(FITC)标记CD4+抗体,藻红朊(PE)标记抗CD8+抗体。取外周血,肝素抗凝,每管50 μ L全血中加入不同荧光素标记的抗体,轻轻混匀后暗室下孵育,然后加入溶血素(OptiLyse)裂解红细胞,轻轻混匀后再次暗室下孵育,经离心、洗涤后流式细胞仪上进行分析。详细步骤见试剂说明书。试剂盒由美国BD公司提供,仪器为美国BECKMAN COULTER公司的Epics XL.MCL流式细胞仪。IgG、IgA、IgM采用免疫散射比浊法测定,仪器为西门子公司的特定蛋白仪,试剂盒由西门子公司提供,详细步骤见试剂说明书。
1.3 统计学处理
2 结果
2.1 2组T淋巴细胞亚群检测结果比较
表1 2组T淋巴细胞亚群检测结果比较(±s)
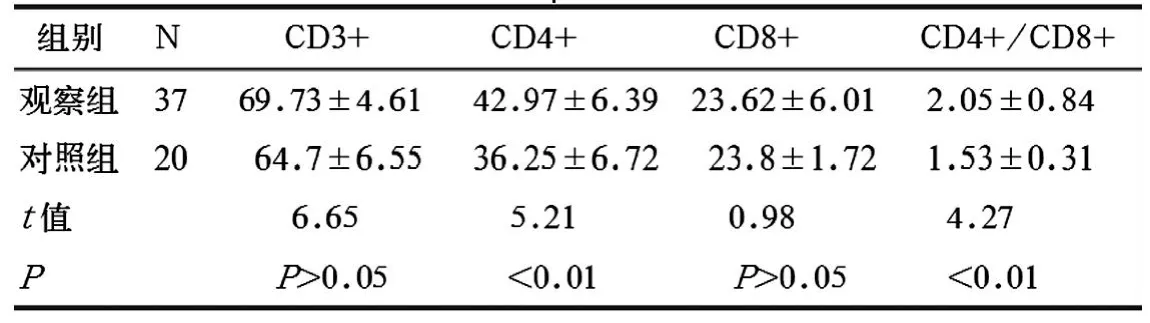
表1 2组T淋巴细胞亚群检测结果比较(±s)
?
同正常对照组比较,观察组患儿外周血CD4+高于对照组(P<0.01),CD4+/CD8+比值高于对照组(P<0.01),CD3+、CD8+2组比较无统计学差异(P>0.05)。见表1。
2.2 2组血清免疫球蛋白水平比较
观察组IgG、IgA、IgM均低于对照组,差异有统计学意义(P<0.01),见表 2。
3 讨论
全球每年约有114亿人发生RV引起的腹泻,并导致大约80万儿童死亡。RV不仅可以引起肠道内感染,而且发病早期即可发生病毒血症并引起全身多器官损害,研究认为可能与RV病毒血症及感染后的免疫损伤有关[3~5],但具体的发病机制还不清楚,还有待于进一步的深入研究。
IgG是血清免疫球蛋白的主要成分,它占总的免疫球蛋白的75%,是初级免疫应答中最持久、最重要的抗体,在抗感染中起到主力军作用,它能够促进单核巨噬细胞的吞噬作用,中和细菌毒素的毒性和病毒抗原结合使病毒失去感染宿主细胞的能力。IgA分血清型和分泌型2种,血清型IgA可介导调理吞噬ADCC作用;分泌型IgA(SIgA)是机体粘膜防御系统的主要成分,是防止病原体入侵机体的第一道防线。研究证明呼吸道、消化道分泌液中SigA含量的高低直接影响粘膜对病原体的抵抗力,两者呈正相关,而IgM是高效能的抗生物抗体[6]。本研究发现观察组IgG、IgA、IgM均低于对照组,差异有统计学意义(P<0.01)。文献报道IgA、IgM较IgG在RV感染时可能发挥更为重要的作用[7]。
T淋巴细胞不仅是机体免疫反应的效应细胞,而且也是重要的免疫调节细胞,机体的免疫平衡的维持依赖于T细胞亚群的相互协调作用,其中CD+4和CD+8T细胞相互诱导,相互制约,形成T淋巴细胞网络,调节机体正常的免疫功能。免疫机制研究发现,免疫缺陷的患儿感染后可在肠道外如肝脏和肾脏等脏器内检测到复制的病毒抗原,这提示肠道外发病机制可能和机体的免疫功能低下有关[8~9]。本研究结果表明RV肠炎合并肠道外感染患儿存在明显的细胞免疫紊乱。与正常对照组相比,虽然总T细胞(CD3+T)没有变化,但CD4+T细胞活化亢进,主要表现为CD4|T淋巴细胞的增高,而CD8+T细胞无变化,相应CD4+/CD8+比值也显著增高,表明CD4+T淋巴细胞增高对机体的免疫反应起到过度辅助作用而产生免疫损伤,这与RV病灶扩散或病程延长存在一定关系。本研究提示在RV感染患儿的治疗中,可适当使用免疫调节剂调节患儿免疫功能和应答,促进病毒的清除,在阻止RV感染后向肠道外播散的过程中可能会有良好效果。
表2 2组血清免疫球蛋白水平比较[(±s),g/L]
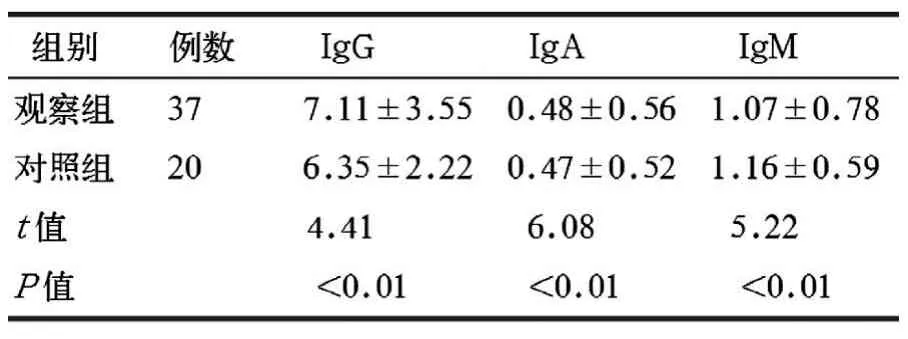
表2 2组血清免疫球蛋白水平比较[(±s),g/L]
?
[1]马晓燕,仲海娟.轮状病毒抗原检验结果189例分析[J].中华现代临床医学杂志,2005,3(20):2158.
[2]王斌,封志纯.重症轮状病毒感染[J].小儿急救医学,2005,12(5):344~345.
[3]魏升云,张淑珍.轮状病毒肠炎研究进展[J].国外医学儿科分册,2004,22(6):409~411.
[4]周瑞,陈兰举,陈名武.轮状病毒感染引起肠道内外发病机制的研究进展[J].国外医学儿科学分册,2005,32(6):354~355.
[5]姚英民,欧乃群,李宁.小儿轮状病毒血症与临床发病特点关系初探[J].中华儿科杂志,2005,43(11):867~869.
[6]郝素珍,王桂琴.实用医学免疫学[M].北京:高等教育出版社,2005,2:15~18.
[7]李建军,刘作义.婴幼儿轮状病毒肠炎的体液免疫功能研究进展[J].实用儿科临床杂志,2004,19(3):176~178.
[8]李宁,姚英民.轮状病毒多系统感染2例分析[J].中华儿科杂志,2002,40:141~143.
[9]姚英民,欧巧群,李宁.小儿轮状病毒血症与临床发病特点关系初探[J].中华儿科杂志,2005,43(11):867~868.
