新型铁改性砂滤料吸附过滤去除水中的磷
2010-06-05吕建波孙力平赵新华李玉友李银磊
吕建波,孙力平,赵新华,李玉友,李银磊,张 磊
(1. 天津大学环境科学与工程学院,天津 300072;2. 天津城市建设学院环境与市政工程系,天津 300384;3. 天津城市建设学院天津市水质科学与技术重点实验室,天津 300384)
新型铁改性砂滤料吸附过滤去除水中的磷
吕建波1,2,孙力平2,3,赵新华1,李玉友2,3,李银磊2,3,张 磊2,3
(1. 天津大学环境科学与工程学院,天津 300072;2. 天津城市建设学院环境与市政工程系,天津 300384;3. 天津城市建设学院天津市水质科学与技术重点实验室,天津 300384)
为进一步提高改性砂滤料对水中磷的去除效果,对现有过滤工艺进行改造,在前期研究的基础上,改进改性方法制备出新型铁改性砂 (IOCS) 滤料,对其进行了扫描电镜(SEM)和X射线衍射(XRD)的表面分析,研究了IOCS对溶液中PO34-的吸附性能和动态过滤再生循环利用.静态吸附实验表明,pH值、接触时间和铁改性砂含量等均会影响IOCS对溶液中PO34-的吸附.25,℃时,Langmuir、Freundlich和Temkin吸附等温线均可较好地拟合铁改性砂对溶液中PO34-的吸附(R2>0.920,0),其拟合曲线的相关性大小顺序为Freundlich>Temkin>Langmuir.由Langmuir吸附等温式得出的IOCS对PO34-的饱和吸附量为0.266 8 mg/g.与同类研究相比,IOCS具有更好的PO34-吸附性能.吸附热力学研究表明,IOCS对PO34-的吸附过程是自发的、吸热的化学过程(ΔG°<0,ΔH°>0).共存阴离子对IOCS吸附PO34-影响的大小顺序为HCO3->SO24->Cl-,但影响不大.过滤再生循环利用实验表明,吸附饱和后IOCS可以使用0.1 mol/L NaOH溶液多次再生重复利用,并保持较高的PO34-去除率,因而可以使用IOCS对现有水和废水处理中过滤除磷工艺进行升级改造.
铁改性砂;吸附;过滤;除磷;再生
磷是引起水体富营养化的重要原因之一,减少饮用水中磷的含量,可以保证饮用水的生物稳定性,因而除磷是水处理工艺的重要目标之一.常见的除磷方法有化学沉淀法(如铝盐、铁盐和钙盐等)、生物法和吸附法.与前2种方法相比,吸附法具有产泥量少、可重复使用和经济高效的优点,并且对去除水中的微量污染物具有独特的优势.因此,吸附法去除水中污染物的研究引起了国内外的广泛关注,所研究的吸附剂主要有赤泥[1-2]、粉煤灰[3-4]、磷灰石[5]、沸石[6]及其他废物材料[7-8]等.
金属(铁、锰、铝等)的氧化物具有良好的吸附性,可用来去除水中的重金属[9-10],但其多呈粉末状,固液分离困难,难以用于水处理中.近年来有研究表明,石英砂等滤料[9,11]表面负载金属氧化物后,对水中的阴离子和阳离子(具有良好的吸附性,同时滤料又可以再生回用.石英砂滤料经氧化物改性后,既保留了石英砂的过滤截留功能,又增加了其对污染物的吸附能力,有利于对现有水处理工艺中滤池的升级改造,因而具有很好的开发潜力,引起了研究者的广泛关注.
目前,国内外对金属氧化物改性砂吸附过滤去除水中PO34-的研究相对较少,许光眉等[18]以Fe(NO3)3·9H2O为改性剂,在110,℃制备成改性砂滤料,研究了其吸附除磷的等温线和热动力学.王俊岭等[19]以三氯化铁溶液为改性剂,将石英砂、石英海砂、陶粒和活化沸石以不同改性方法制备成改性滤料,进行过滤去除水中微量磷的研究,发现500,℃制备的改性石英砂对总磷的去除效果最好.Arias等[13]使用硝酸铁和三氯化铝溶液对粉末石英砂进行改性,制备成铁改性砂和铝改性砂,研究了2种改性砂对水中PO34-的吸附及其解吸性能,发现铝改性砂对PO34-具有更好的吸附去除效果.
在这些研究中,铁改性砂对磷的吸附去除性能仍然较低,以除磷为目标的高效铁改性砂滤料有待于进一步研制开发.笔者在前期研究的基础上[20],通过改进改性石英砂的制备方法,自制出以除磷为目标的高效能新型铁改性石英砂(iron-oxide-coated sand, IOCS)滤料,对铁改性砂滤料吸附过滤除磷和再生循环利用进行了研究,取得了良好的效果.
1 材料与方法
1.1 铁改性砂滤料的制备
石英砂滤料经筛分后用自来水反复冲洗干净后,置于100~110,℃烘箱中烘干,然后用0.1,mol/L稀盐酸溶液浸泡24,h后,再用蒸馏水冲洗干净,于烘箱中烘干后用于改性.改性步骤如下:将浓度2.5,mol/L FeCl3·6H2O溶液400,mL与1,mL,10,mol/L NaOH溶液混合,将混合溶液与上述800,mL石英砂混合,并搅拌均匀后,置于干燥箱中于110,℃烘96,h以上,间歇搅拌至干;然后在200,℃下烘干,冷却后用水冲洗干净后,在110,℃下烘干.经上述改性步骤后得到的滤料即为铁改性砂.
1.2 静态吸附实验
静态吸附实验主要研究了pH值、接触时间和铁改性砂含量对其吸附PO34-的影响,并进行了吸附等温线和热力学及溶液中共存阴离子(Cl-、SO24-、HCO-3)对吸附的影响研究.为减少滤料粒径差异对吸附的影响,实验中采用的铁改性砂滤料粒径为0.8~0.9,mm.含磷原水用KH2PO4和去离子水配制.所有吸附实验均在150,mL锥形瓶中进行,含磷原水体积均为50,mL.通过水浴振荡器控制温度,振荡速度为120,r/min.用硝酸和NaOH溶液调节pH值,背景电解质为0.01,mol/L的NaNO3溶液,所有吸附实验均重复2次,取平均值进行数据分析.
1.3 动态过滤及再生实验
动态过滤除磷效果及滤柱能否再生循环利用影响到铁改性砂滤料的实用性.本实验中,滤柱直径为25,mm,底部装有4,cm高的级配卵石,铁改性砂滤料高35,cm,粒径0.7~1.2,mm.含磷原水浓度为1.2,mg/L,由KH2PO4和自来水配制,通过蠕动泵调节流速为23,mL/min,以下向流方式进行过滤.每次过滤运行时间为7,h,然后使用0.1,mol/L,NaOH溶液进行上向流解吸再生实验,30,min后,用自来水反洗3,min,流速均为40,mL/min.动态过滤及再生循环利用实验连续进行3次.
1.4 试剂与测定方法
实验用试剂主要有:KH2PO4(优级纯)、HNO3(分析纯)、NaOH(分析纯)和FeCl3·6H2O(分析纯).
测定方法均为标准法,pH值采用Micro-processor pH计测定;4PO3-浓度采用钼锑抗分光光度法测定(岛津UV-VIS 2550紫外可见分光光度计);铁改性砂表面负载铁含量采用Perkin Elmer公司的Analyst 800原子吸收光谱仪测定,测定步骤为:准确称取1,g铁改性砂,于1∶1盐酸中,在150,℃下加热消解,待显出石英砂的本色后,停止消解并冷却,经滤纸过滤定容进行测定,同时做3个平行样取平均值.
2 结果与讨论
2.1 铁改性砂表面特征分析
由于铁氧化物在石英砂表面的黏附,改性砂滤料表面的物理化学性质会发生变化,为此,本研究对改性滤料进行了表面铁含量测定、扫描电镜(scanning electron microscopy,SEM)及X射线衍射(X-ray diffraction spectroscopy,XRD)的表面成分分析.
经测定,铁改性砂表面铁含量为31.13,mg/g,石英砂经改性后负载有金属氧化物,因而可以增强其吸附性.酸碱抗性实验表明,铁改性砂具有较好的稳定性.
石英砂及改性砂的扫描电镜照片表明,石英砂表面光滑均匀没有棱角,表面具有一定的沟槽与凹坑,容易让金属氧化物附着.而铁改性砂表面明显粗糙,孔隙更多,比表面积大,且附有大量的晶体,经X射线衍射(图1)分析表明,所含物质除SiO2外,铁改性砂所含氧化物主要是针铁矿(FeO(OH))、磁铁矿(Fe3O4)和赤铁矿(Fe2O3).

图1 铁改性砂的XRD图谱Fig.1 XRD spectra of IOCS
2.2 铁改性砂吸附磷的影响因素
2.2.1 初始pH值的影响
溶液pH值是影响固液界面4PO3-吸附的重要因素.本实验中,4PO3-初始浓度为5.5,mg/L,接触时间为24,h,温度为25,℃,铁改性砂含量为20,g/L.不同初始pH值(2.4~9.5)对铁改性砂吸附磷的影响见图2.可见,随着pH值的增加,铁改性砂对4PO3-的吸附量呈降低趋势,且降低较平缓.已有研究表明[21-22],pH值约为4~10时,赤铁矿、γ-Al2O3和铝土矿等对4PO3-吸附随着pH值的增加逐渐降低,可见,本研究的实验结果与已有研究的结论类似.
同时可以看出,铁改性砂对4PO3-的去除率保持在62%~84%,说明在较宽的pH值范围内,铁改性砂对4PO3-保持较高的去除率,受原水pH值的影响较小,有利于在实际工程中应用.由于实际应用时水和废水的pH值一般在中性附近,因而后续研究在pH值为6.8±0.1时进行.
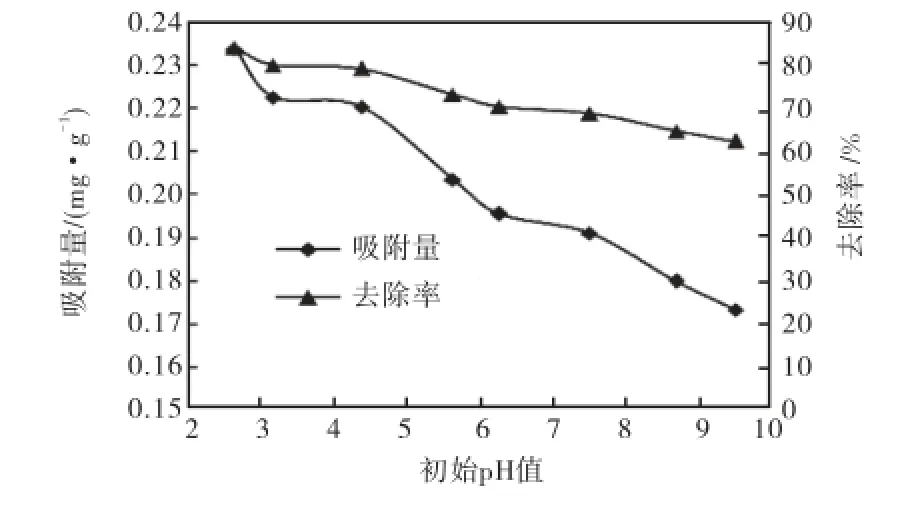
图2 初始pH值对铁改性砂吸附PO34-的影响Fig.2 Effect of initial pH on PO34-adsorption on IOCS
2.2.2 接触时间的影响
接触时间对铁改性砂吸附PO34-的影响见图3,PO34
-初始浓度为5.14,mg/L,铁改性砂含量为80,g/L,温度为20,℃.可见,铁改性砂对PO34-的去除率随着接触时间的增加而逐渐增加,铁改性砂对PO34-的吸附在约200,min时达到平衡,对PO34-的吸附速率较快,其后,铁改性砂对PO34-的吸附变化趋势比较平缓,经较长的时间后,对PO34-的吸附达到稳定.

图3 接触时间对铁改性砂吸附PO43-的影响Fig.3 Effect of contact time on PO34-adsorption on IOCS
2.2.3 铁改性砂含量的影响
铁改性砂含量对溶液中PO34-吸附的影响见图4,PO34-初始浓度为2.2,mg/L,接触时间为24,h,温度为20,℃.可见,当PO34-初始浓度一定时,铁改性砂对溶液中PO34-的去除率随着铁改性砂量的增加而迅速增加,直至铁改性砂含量达到20,g/L.PO34-去除率增加的主要原因可能是铁改性砂含量的增加提供了更多的吸附表面积,因此提高铁改性砂的浓度有助于对溶液中PO43-去除率的提高.此后,去除率增加变缓,直至去除率达到最大值,这与Gupta等[23]用铁改性砂对溶液中As(Ⅲ)进行吸附的实验结果类似.
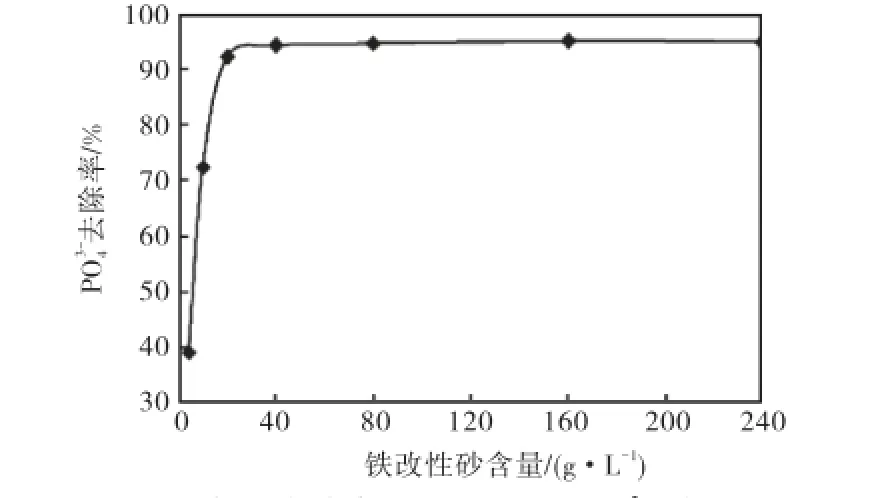
图4 铁改性砂含量对其吸附PO34-的影响Fig.4 Effect of IOCS dose on PO34-adsorption
2.3 铁改性砂的吸附等温线
等温吸附实验中,4PO3-初始浓度范围为0.6~14,mg/L,铁改性砂含量为20,g/L,接触时间为24,h,温度分别为15,℃、25,℃和35,℃.对于固液体系的吸附行为,常用如下吸附等温方程式来进行描述[24].

式中:q为吸附平衡时的PO34-吸附量,mg/g;qm为PO34
-饱和吸附量,mg/g;C为吸附平衡时溶液中PO34-的浓度,mg/L;b、K、n、A和B均为常数,可通过实验数据经回归分析后求出.
本研究中铁改性砂对PO34-的吸附等温线见图5.图5表明了不同PO34-平衡浓度时铁改性砂的吸附行为.经对Langmuir方程式和Freundlich方程式数学变换后,分别得到线性关系式

25,℃时,Langmuir、Freundlich和Temkin等温线的线性图解见图6.通过线性求解得出的铁改性砂对溶液中4PO3-吸附的等温方程式的各常数及相关系数见表1.可见,各吸附等温式的相关系数均较高(R2>0.920,0),铁改性砂对溶液中PO34-吸附的拟合曲线的相关性大小顺序为Freundlich>Temkin> Langmuir,Langmuir、Freundlich和Temkin吸附等温线均可较好地拟合铁改性砂对溶液中PO34-的吸附.虽然吸附等温线拟合数据在数据分析方面有重要意义,但并不能说明铁改性砂的实际吸附机理.
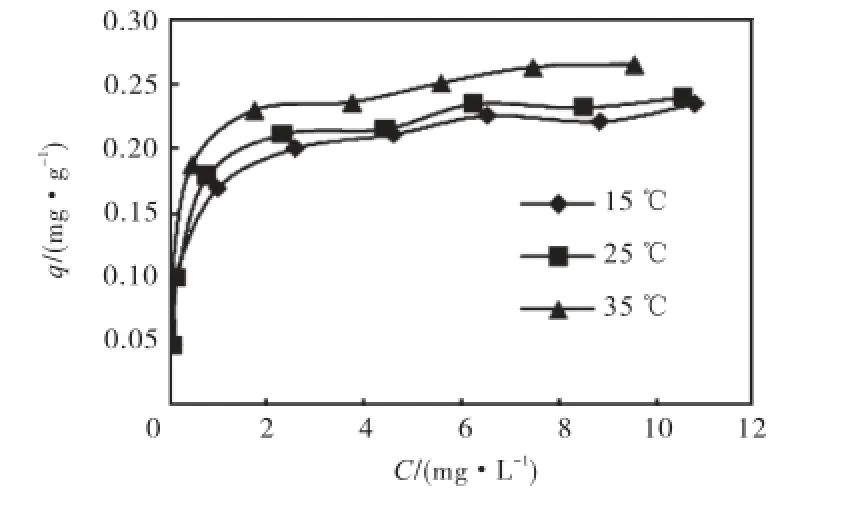
图5 不同温度下铁改性砂对PO34-的吸附等温线Fig.5 Adsorption isotherms of PO43-on IOCS at various temperatures

图6 铁改性砂吸附PO34-的等温线 (25 ℃)Fig.6 Langmuir, Freundlich and Temkin isotherms for adsorption of PO34-on IOCS(25 ℃)
由表1中Freundlich吸附等温式常数可以看出,1<n<10,说明铁改性砂对PO34-的吸附属于有利吸附[13].由Langmuir吸附等温式得出的铁改性砂对PO34-的饱和吸附量为0.266,8,mg/g,不同文献中提到的铁改性砂对溶液中PO34-的Langmuir饱和吸附量比较见表2.可见,与国内的研究者相比,笔者所得铁改性砂滤料对PO34-的吸附效果明显提高,Arias等[13]的研究中,虽然石英砂的吸附量很大,但因其呈粉末状,不适宜在滤池改造时用作滤料.
综上所述,与其他同类研究相比,笔者在前期研究的基础上,改进制备方法后,在制备温度和单位砂量所用改性剂量较低的条件下,制备出的新型铁改性砂对溶液中4PO3-的吸附量大大增加,吸附速度快,去除率高,是性价比高的改性滤料.

表1 铁改性砂吸附PO34-的等温线常数(25,℃)Tab.1 Langmuir,Freundlich and Temkin isotherms constants for PO34-adsorption on IOCS (25,℃)

表2 不同铁改性砂吸附PO34-的Langmuir饱和吸附量比较Tab.2 Comparison of Langmuir adsorption capacity of dif-Tab.2 ferent IOCS for PO34-at different coating processes
2.4 吸附热力学
为说明铁改性砂吸附PO34-过程中温度对吸附热力学参数的影响,需要确定吸附的标准吉布斯函数变ΔG °、标准焓变ΔH°和标准熵变ΔS°等热力学参数.标准吉布斯函数变[8]

式中:R为气体常数,8.314×10-3kJ/(mol·K);T为绝对温度,K;b为温度T时的吸附平衡常数.
确定标准焓变HΔ°和标准熵变SΔ°的关系式为[8]

可见,ln b与T−1呈线性关系,图7给出了ln b与T−1关系的范特霍夫(Van′t Hoff)公式的线性图解,其斜率为−ΔH°/R,截距为ΔS°/R,从而可以求出ΔH°和ΔS°.不同温度下铁改性砂吸附PO34-的热力学参数见表3.
从表3可以看出,ΔG°为负值,说明吸附过程可以自发进行,随着温度升高,ΔG°减少,说明高温有利于吸附反应的进行.ΔH°为正值,说明铁改性砂吸附PO34-为吸热反应.ΔS°为正值,说明PO34-吸附过程中固液界面的混乱度增加.
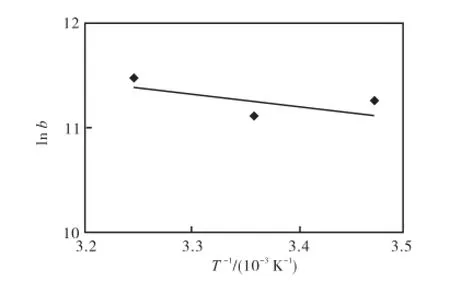
图7 铁改性砂吸附PO43-的范特霍夫公式线性图解Fig.7 Van′t Hoff plot for the adsorption of PO34-on IOCS
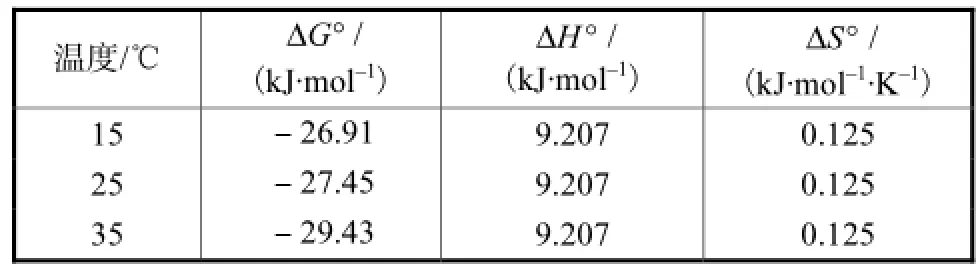
表3 不同温度下IOCS对PO34-吸附的热力学参数Tab.3 Thermodynamic parameters for the adsorption of PO34-on IOCS at various temperatures
2.5 共存阴离子对IOCS吸附PO43-的影响
铁改性砂吸附PO34-过程中,溶液中共存阴离子(SO24
-、Cl-、HCO-3等)可能会与PO34-产生竞争吸附,不利于实际应用时铁改性砂对PO34-的吸附.本实验中,PO34-初始浓度为5.5,mg/L,铁改性砂含量为20,g/L,接触时间为24,h,温度为25,℃,不同浓度SO2-、Cl-、HCO-对铁改性砂吸附PO3-的影响结果见
4
34图8.
由图8可见,随着3种阴离子浓度的增加(0~300, mg/L), 铁改性砂对PO34-的去除率总体上呈降低趋势,3种阴离子对PO34-吸附影响的大小顺序为:HCO-3>SO24->Cl-,Cl-对PO34-的去除率影响很小.同时可以看出,3种阴离子在较宽的浓度范围内,对铁改性砂吸附4PO3-的影响不大,说明3种阴离子在铁改性砂上的吸附均比4PO3-弱,有利于铁改性砂在实际中的应用.

图8 共存阴离子对IOCS吸附PO43-的影响Fig.8 Effects of competitive anions on the adsorption of Fig.8 PO34-on IOCS
2.6 PO4
3-吸附前后的铁改性砂EDAX分析
PO34
-吸附前后铁改性砂的元素组成EDAX分析采用X射线能谱仪(Oxford Inca Energy,300)进行测定,测定的谱图结果见图9.可见,除了石英砂原有的C、Si和O等元素外,改性后石英砂表面因附有铁的氧化物,故均观察到Fe的存在.吸附后铁改性砂同时观察到P的存在,从而直接证明铁改性砂对PO34-的吸附作用.

图9 吸附PO43-前后IOCS的EDAX谱图Fig.9 EDAX spectrum of IOCS without and with PO43-adsorption
2.7 动态过滤及再生循环利用
动态过滤除磷及再生循环利用实验结果见图10.可见,连续3次过滤实验中,铁改性砂吸附过滤均保持较高的4PO3-去除率,运行时间7,h内的平均去除率均在50%以上.使用0.1,mol/L NaOH溶液可以对吸附后铁改性砂滤料进行解吸再生,再生过程出水磷浓度变化见图11.可见,在较短的再生时间内(约5~10,min),再生液出水磷浓度即达到峰值,大大高于原水磷浓度1.2,mg/L,再生时间超过30,min以后,再生液出水磷浓度已较低,难以进一步解吸,铁改性砂表面的磷基本解吸完毕,其吸附除磷能力得到恢复,可以进行循环利用.
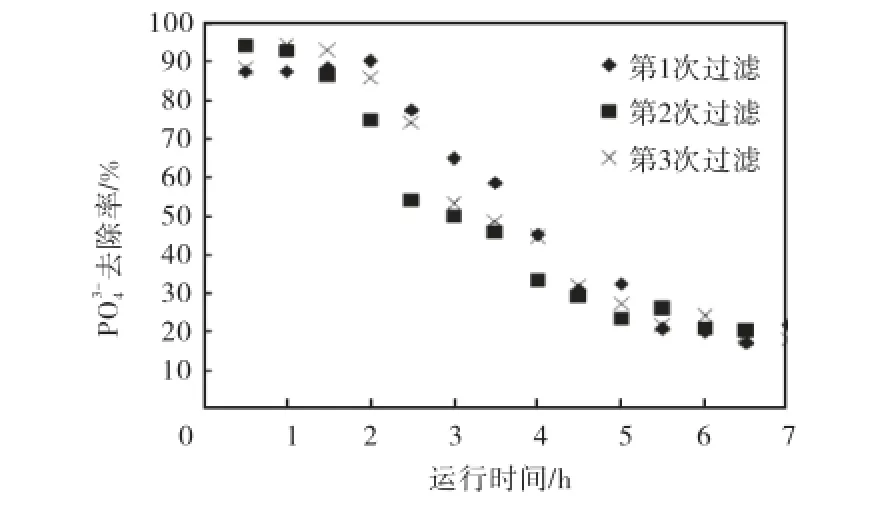
图10 连续3次过滤除磷效率对比Fig.10 Comparison of phosphate removal during all three cycles

图11 再生过程出水磷浓度变化Fig.11 Phosphate concentration of effluents with regeneration time
2.8 铁改性砂除磷机理探讨
国内外研究者对IOCS除磷已进行了相关研究[8,12-13,18-20].普通石英砂pHZPC(pH of zero point of charge,零电荷点pH)一般为0.7~2.2,而铁改性砂因表面附有铁氧化物,其pHZPC一般为8.3~10.3,当溶液pH<pHZPC时,铁改性砂表面带有正电荷,因而有利于对溶液中磷酸根等阴离子或带负电荷颗粒的吸附.但由于不同研究者在改性过程中采用改性剂种类、单位砂量所用改性剂量、改性温度、pH值、改性时间和次数等的不同,从而使石英砂负载的金属含量和氧化物类型不同,所得改性砂的吸附性能不同.本研究中,笔者通过改进IOCS的制备方法,在低温条件下(200,℃)制备出新型铁改性砂滤料,表面附有针铁矿(FeO(OH))、磁铁矿(Fe3O4)和赤铁矿(Fe2O3)等金属氧化物,而前期研究中[20]高温条件下(550,℃)制备的IOCS,其表面金属氧化物主要是赤铁矿(Fe2O3).有关铁氧化物的研究已经表明[25-26],针铁矿(FeO(OH))对溶液中磷的吸附能力大于赤铁矿(Fe2O3),这可能是低温条件下制备的新型铁改性砂对溶液中磷有更好的吸附性的主要原因.
在酸性或中性条件下,溶液中磷主要以H PO-24和HPO2-存在,铁改性砂表面的铁氧化物会发生羟基4化(用SOH表示羟基化氧化物),其吸附反应方程式为[27]
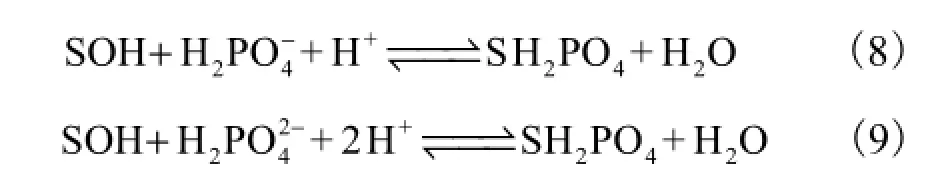
当磷被吸附时,反应向右进行,而用NaOH溶液进行解吸再生时,发现溶液pH值随解吸的进行有降低趋势,说明反应向左进行,吸附在铁改性砂表面的磷被解吸下来.可见,铁改性砂对溶液中磷的吸附除静电吸附外,还可能存在离子交换吸附.
3 结 论
(1) 制备的新型铁改性砂表面的铁含量为31.13,mg/g,XRD分析表明,所含物质除SiO2外,表面负载的金属氧化物主要是针铁矿(FeO(OH))、磁铁矿(Fe3O4)和赤铁矿(Fe2O3).
(2) pH值、接触时间和铁改性砂含量等均会影响其对溶液中PO34-的吸附.25,℃时,Langmuir、Freundlich和Temkin吸附等温线均可较好地拟合铁改性砂对溶液中PO34-的吸附.其拟合曲线的相关性大小顺序为Freundlich>Temkin>Langmuir.由Langmuir吸附等温式得出的铁改性砂对PO34-的饱和吸附量为0.266,8,mg/g,与其他同类研究相比,吸附性能大大提高.
(3) 吸附热力学研究表明,铁改性砂对PO34-的吸附过程是自发的、吸热的化学过程.
(5) 铁改性砂对溶液中磷的吸附除静电吸附外,还可能存在离子交换吸附.
研究结果表明,新型铁改性砂滤料对溶液中PO34-具有良好的吸附性,材料成本低,经实验表明可多次再生重复利用,具有环境友好性,因而可以用于现有水和废水处理中过滤除磷工艺的升级改造.
[1] Liopez E,Soto B,Arias M,et al. Adsorbent properties of red mud and its use for wastewater treatment[J]. Water Research,1998,32(4):1314-1322.
[2] Pradhan J,Das J,Das S N,et al. Adsorption of phosphate from aqueous solution using activated red mud[J]. Journal of Colloid and Interface Science,1998,204(1):169-172.
[3] Weng C H,Huang C P. Adsorption characteristics of Zn(Ⅱ)from dilute aqueous solution by fly ash[J]. Colloids Surf A:Physicochem Eng Aspects,2004,247 (1/2/3):137-143.
[4] Oguz E. Sorption of phosphate from solid/liquid interface by fly ash[J]. Colloids Surf A:Physicochem Eng Aspects,2005,262(1/2/3):113-117.
[5] Kandah M L. Zinc and cadmium adsorption low-grade phosphate[J]. Sep Purif, Technol,2004,35(1):61-70.
[6] Tillman F D,Bartelt-Hunt S L,Craver V A,et al. Relative metal ion sorption on natural and engineered sorbents:Batch and column studies[J]. Environ Eng Sci,2005,22(3):400-409.
[7] Agyei N M,Strydom C A,Potgieter J H. The removal of phosphate ions from aqueous solution by fly ash,slag,ordinary Portland cement and related blends[J]. Cem Concr Res,2002,32(12):1889-1897.
[8] Boujelben N,Bouzid J,Elouear Z,et al. Phosphorus removal from aqueous solution using iron coated natural and engineered sorbents[J]. Journal of Hazardous Materials,2008,151(1):103-110.
[9] Benjamin M M,Sletten R S,Bailey R P,et al. Sorption and filtration of metals using iron-oxide-coated sand[J]. Water Research,1996,30(11):2609-2620.
[10] Villasenor G N,Strathmann T J. Ferrous iron sorption by hydrous metal oxides[J]. Journal of Colloid and Interface Science,2006,297(2):443-454.
[11] 邓慧萍,梁 超,常 春,等. 改性滤料和活性炭去除有机物的特性研究[J]. 同济大学学报,2006,34(6):766-769. Deng Huiping,Liang Chao,Chang Chun,et al. A characteristic study of coated filter media and activated carbon in removing organic matter[J]. Journal of Tongji University,2006,34(6):766-769(in Chinese).
[12] Ayoub G M,Koopman B,Pandya N. Iron and aluminum hydroxy(oxide)coated filter media for low concentrationphosphorous removal[J]. Water Environ Res,2001,73 (4):478-485.
[13] Arias M,Silva-Carballal J D,García-Ríoc L,et al. Retention of phosphorus by iron and aluminum-oxides-coated quartz particles[J]. Journal of Colloid and Interface Science,2006,295(1):65-70.
[14] Thirunavukkarasu O S,Viraraghavan T,Suvramanian K S. Arsenic removal from drinking water using iron oxidecoated sand[J]. Water,Air,and Soil Pollution,2003,142(1/2/3/4):95-111.
[15] Han R,Zou W,Zhang Z,et al. Removal of copper(II)and lead(II)from aqueous solution by manganese oxide coated sand(I):Characterization and kinetic study[J]. Journal of Hazardous Materials,2006,137(1):384-395.
[16] Han R,Zou W,Li H,et al. Copper(II)and lead (II) removal from aqueous solution in fixed-bed columns by manganese oxide coated zeolite[J]. Journal of Hazardous Materials,2006,137(2):934-942.
[17] Hu P Y,Hsieh Y H,Chen J C,et al. Characteristics of manganese-coated sand using SEM and EDAX analysis [J]. Journal of Colloid and Interface Science,2004,272(2):308-313.
[18] 许光眉,施 周,邓 军. 石英砂负载氧化铁吸附除磷的热动力学研究[J]. 环境工程学报,2007,1(6):15-18. Xu Guangmei,Shi Zhou,Deng Jun. Thermodynamic and kinetic investigation of phosphate adsorption on iron oxide coated sand[J]. Chinese Journal of Environmental Engineering,2007,1(6):15-18(in Chinese).
[19] 王俊岭,冯萃敏,龙莹洁,等. 改性石英砂过滤吸附去除微量磷[J]. 水处理技术,2007,33(12):70-72. Wang Junling,Feng Cuimin,Long Yingjie,et al. Performance of absorption and filtration of iron oxide coated-sand for phosphorus removal[J]. Technology of Water Treatment,2007,33(12):70-72(in Chinese).
[20] 吕建波,孙力平,赵新华,等. 涂铁砂滤料吸附过滤去除城市污水厂二级处理出水中磷的研究[J]. 水处理技术,2009,35(3):31-34. Lu˙˙ Jianbo,Sun Liping,Zhao Xinhua,et al. Phosphate removal from municipal secondary effluent by iron-oxidecoated sand adsorption and filtration[J]. Technology of Water Treatment,2009,35(3):31-34(in Chinese).
[21] Horanyi G,Joo P. Some peculiarities in the specific adsorption of phosphate ions on hematite and γ-Al2O3as reflected by radiotracer studies[J]. Journal of Colloid and Interface Science,2002,247(1):12-17.
[22] Altundogan H S,Tumen F. Removal of phosphates from aqueous solutions by using bauxite(I):Effect of pH on the adsorption of various phosphates[J]. J Chem Tech Biotechnol,2001,77(1):77-85.
[23] Gupta V K,Saini V K,Jain N. Adsorption of As(Ⅲ) from aqueous solutions by iron oxide-coated sand[J]. Journal of Colloid and Interface Science,2005,288(1):55-60.
[24] Mead J A. Comparison of the Langmuir,Freundlich and Temkin equations to describe phosphate adsorption properties of soils[J]. Aust J Soil Res,1981,19(3):333-342.
[25] Arai Y,Sparks D L. ATR-FTIR spectroscopic investigation on phosphate adsorption mechanisms at the ferrihydrite-water interface[J]. Journal of Colloid and Interface Science,2001,241(2):317-326.
[26] 谢晶晶,庆承松,陈天虎,等. 几种铁(氢)氧化物对溶液中磷的吸附作用对比研究[J]. 岩石矿物学杂志,2007,26(6):535-538. Xie Jingjing,Qing Chengsong,Chen Tianhu,et al. A comparison of phosphate adsorption capacity between different iron hydroxides/oxides[J]. Acta Petrologica et Mineralogica,2007,26(6):535-538(in Chinese).
[27] Sutha K,Mohammad F A,Khemarath O,et al. Copper,chromium,and arsenic adsorption and equilibrium modeling in an iron-oxide-coated sand,background electrolyte system[J]. Water,Air,and Soil Pollution,2000,119(1/ 2/3/4):105-120.
Adsorption Removal of Phosphate from Aqueous Solution Using a New Type of Iron-Oxide-Coated Sand Filter Media
LÜ Jian-bo1,2,SUN Li-ping2,3,ZHAO Xin-hua1,LI Yu-you2,3,LI Yin-lei2,3,ZHANG Lei2,3
(1. School of Environmental Science and Technology,Tianjin University,Tianjin 300072,China;2. Department of Environmental and Municipal Engineering,Tianjin Institute of Urban Construction,Tianjin 300384,China;3. Tianjin Key Laboratory of Water Quality Science and Technology,Tianjin Institute of Urban Construction,Tianjin 300384,China)
In order to enhance phosphate removal from aqueous solution using iron-oxide-coated sand (IOCS)filter media,a new type of IOCS was prepared by improving coating process based on the previous study. The adsorbability of phosphate on IOCS,and the possibility of regeneration and reuse of phosphate adsorbed IOCS were investigated. Scanning electron microscopy(SEM)and X-ray diffraction spectroscopy(XRD)were used to observe the surface properties and morphology of the coated layer. Effects of pH,contact time and dose of IOCS on phosphate removal were studied in batch experiments. Three isotherm equations(Langmuir,Freundlich and Temkin)were used for data fitting. The results showed that the data obtained from isotherm experiments(at the temperature of 25,℃)could be well described using the three isotherm equations,with the correlation coefficients2R>0.920,0. The phosphate adsorption capacity of IOCS obtained from Langmuir fitting data was 0.266 8 mg/g. Compared with the IOCS in other studies of the same kind,the IOCS in this study has higher adsorption capacity for phosphate. The results of adsorptionthermodynamics of phosphate by IOCS indicate that the adsorption of phosphate on IOCS is spontaneous(ΔG°<0)and endothermic(ΔH°>0). The sequence of anions studied affecting the adsorption of phosphate on IOCS is HCO3->SO24->Cl-,but their effect was not obvious. Column experiments indicate that IOCS has a high phosphate removal rate,and saturated IOCS can be regenerated effectively by 0.1,mol/L NaOH solution. This study demonstrates that IOCS can be used as an alternative filter media for water and wastewater treatment without any side effect or treatment process alternation.
iron-oxide-coated sand;adsorption;filtration;phosphate removal;regeneration
X703.1
A
0493-2137(2010)12-1115-08
2009-06-23;
2010-01-15.
国家自然科学基金资助项目(50808128);巢湖流域城市水污染控制及水环境治理技术研究与综合示范资助项目(2008ZX07316);国家水体污染控制与治理科技重大专项资助项目(2008ZX07314-003).
吕建波(1976— ),男,博士,讲师,jianbo98@126.com.
孙力平,slpyqs@vip.sina.com.
