大亚湾表层沉积物中磷的形态分布特征*
2010-06-05余汉生方宏达
何 桐,谢 健,余汉生,方宏达
(1.国家海洋局南海海洋工程勘察与环境研究院,广东 广州 510300;2.国家海洋局南海环境监测中心,广东 广州 510300)
海洋中的磷作为重要的生源要素,不仅直接影响着海洋的初级生产力,而且磷与碳的关系密切,对海洋碳循环的影响巨大,直接与全球气候变化和全球生态环境变化相关[1]。近年来,特别是IGBP核心计划JGOFS、GLOBEC、LOICZ、SOLAS等实施以来,对磷的生物地球化学有了系统深入的了解,具体体现在磷与海洋生物泵的关系,以及碳-氮-磷的耦合特征等方面,这些研究为深入研究磷的生态学功能奠定了基础[2]。
海洋沉积物是海洋环境中磷的重要蓄积库,它不仅对上覆水体中磷含量有一定的缓冲作用,而且也是海水中磷的重要来源之一[3-5]。磷能否与沉积物发生界面交换取决于其形态,不同结合态的磷具有不同的地球化学行为和生物有效性,只有某些形态的磷,在物理化学及生物学等因素的作用下,通过解吸、溶解、还原等过程而释放到水中,转化为生物可直接利用的磷,成为影响水域营养状况及诱发富营养化的重要因素[6]。因此,对沉积物中磷的地球化学形态的研究,有助于了解海水中磷的动态循环以及在沉积物-水界的迁移转化和随后的成岩作用等地球化学行为,具有重要的环境地球化学意义。
大亚湾位于南海北部,约114°30′~114°50′E,22°30′~22°50′N之间。西邻香港,东接红海湾,海岸线长约92 km,面积600多km2,平均水深约10 m,水交换差[7]。大亚湾内生物资源丰富、生境多样,是广东省的水产资源繁殖保护区[8]。目前,对大亚湾磷的研究主要集中在水体及沉积物-海水界面的交换速率及通量等方面[9-13],但对大亚湾沉积物中磷尤其是磷的形态及生物可利用性研究则鲜有报道[14]。本文首次采用SEDEX法将大亚湾表层沉积物中不同形态的磷分离开,继而分析表层沉积物中不同形态磷的含量、分布特征、影响因素及生物可利用性,为进一步地认识大亚湾生源要素磷的生物地球化学循环规律提供参考。
1 材料与方法
1.1 样品采集及处理
在大亚湾海域设置13个调查站位(图1),于2007年8月对其进行了一个航次的调查,采集上覆水和表层沉积物。上覆水使用有机玻璃采水器采集,将其装于聚乙烯瓶中冷藏保存。表层沉积物使用蚌式采泥器进行采集,收集0~5 cm沉积物于聚乙烯塑料袋中,密封置于冰箱带回实验室进行分析。沉积物样品经冷冻干燥后,用木棒分散、研磨、过筛(80目)后,置于密封袋中,保存于低温冰箱中备用。

图1 大亚湾表层沉积物采样站位及TP、IP、OP的空间分布
1.2 沉积物中磷形态分析方法
准确称取0.2 g的干沉积物样品,采用Ruttenberg[15]的分级浸取程序(SEDEX)进行分析测定,得到沉积物中的4种无机形态磷:吸附态磷Ads-P(adsorbed-bound phosphorus)、铁结合态磷Fe-P(iron-bound phosphorus)、自生磷灰石及钙结合态磷Ca-P(authigenic carbonate fluorapatite + biogenic apatite + CaCO3-associated phosphorus)及碎屑态磷De-P(detrital apatite phosphorus),其逐级提取过程概括于图2。浸取液中的磷含量均采用流动注射分析仪(LACHAT QC8500,美国)分析,测定的基本原理见《海洋监测规范》(GB17378.4-1998)。
总磷TP、无机磷IP及有机磷OP的测定方法参见文献[16]。其它环境参数的测定均参照《海洋监测规范》(GB17378.4-1998)中规定的方法。
1.3 数据处理方法
实验数据采用Origin7.5、Surfer8.0等软件进行统计分析和插图制作。空间插值采用普通Kriging插值法。
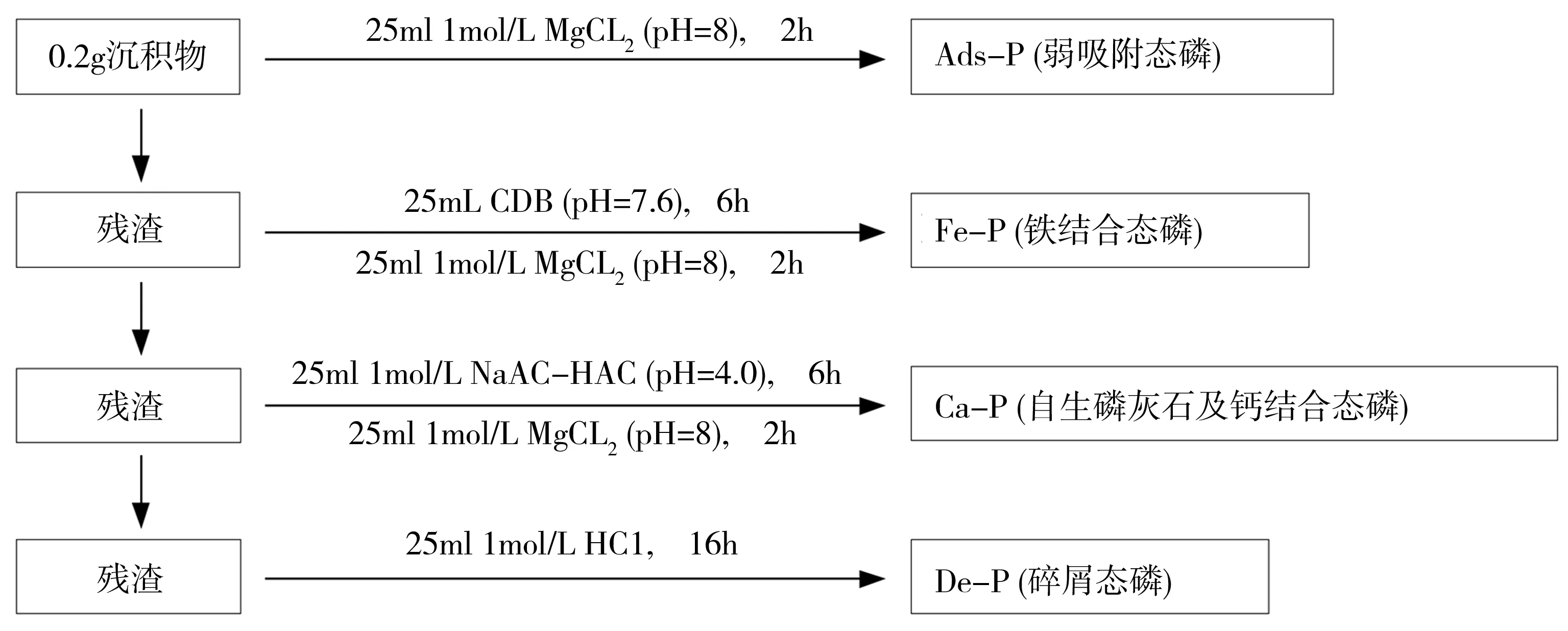
图2 无机形态磷的逐级提取流程图
2 结果与讨论
2.1 表层沉积物中磷的含量与分布
大亚湾表层沉积物中各形态磷含量的统计结果列于表1。沉积物中TP划分为IP和OP,而IP又划分为Ads-P、Fe-P、Ca-P和De-P四大类。
2.1.1 沉积物中总磷的含量及空间分布 TP的含量在286.58~386.75 mg/kg之间,平均含量为341.87 mg/kg(表1),其中含量的最大值出现在哑铃湾内的DS12,含量最小值出现在湾口东侧的DS26。大亚湾TP含量低于何清溪等[14]的研究结果,与岳维忠等[17]在珠江口的研究结果相近。由于区域海洋环境的异同和变化,加之所采用研究方法的不同,是造成含量研究结果差异的主要原因。TP的空间分布整体呈现出湾西部高于东部的分布趋势(图1),造成这种分布趋势的主要原因:一是湾西部人类活动频繁,污染源相对较多;二是湾西部沉积物中粘土级含量高于东部[18],对磷的吸附能力强。
2.1.2 无机磷和有机磷的含量及空间分布 IP的含量范围为251.06~333.05 mg/kg,平均含量为290.81 mg/kg(表1),占TP含量的80.68%~91.52%,平均为85.11%,是沉积磷的主要赋存形态。沉积物中OP的含量在29.71~71.94 mg/kg之间,平均含量为51.05 mg/kg(表1),占TP含量的8.48%~19.32%,平均为14.89%。IP含量的最大值出现在哑铃湾内DS12,其次为DS25和DS19,其余绝大多数都在280 mg/kg左右(图1)。此外,OP的变异系数相对IP较大,这在一定意义上反映出OP对海湾环境变化更具敏感性。IP、OP空间分布的整体趋势与TP相似(图1)。

表1 大亚湾表层沉积物中各形态磷统计分析结果1)
1) TP、IP、OP的样本数为13,其它无机形态磷的样本数为5
2.1.3 无机形态磷的组成、分布和变化 对各站位表层沉积物中无机形态磷进行化学连续分级提取,其结果见表1和图3。可知,沉积物中Ads-P含量最低,占IP含量的6.18%~8.24%;其次是Fe-P,占IP含量的9.49%~11.13%;再次是Ca-P,占IP含量的32.52%~37.23%;沉积物中De-P的含量最高,在114.85~152.29 mg/kg之间,占IP含量的46.15%~50.08%。由此可见,De-P是沉积物中IP的主要存在形态,这与北部湾的研究结果是一致的[19]。此外,Ads-P的变异系数较大,这在一定意义上反映出这种形态磷较其它三种形态更易受海洋环境变化的影响,表明此种形态磷的地球化学活性大,易于在沉积物-海水界面间迁移转化和被水生植物吸收利用。从空间分布上看,各无机形态磷在DS12站位的沉积物中含量均较高,与TP、IP相似;同一形态无机磷在其它四个站位的沉积物中含量相差不大(图3)。

图3 大亚湾表层沉积物中无机形态磷的空间分布
2.2 沉积物中磷的形态特征与环境因子的关系
弱吸附态磷(Ads-P)的主要载体是沉积物中的氧化物、氢氧化物以及粘土矿物颗粒等,主要源于水生颗粒。物化条件如温度、pH、水动力条件、生物扰动、氧化还原环境特征等因素都可导致这种形态的磷向水体释放,从而对上覆水体的营养状况有着一定的影响[20]。从Ads-P与其它磷形态的相关分析中可以看出(表2),Ads-P与沉积物中的Fe-P(r=0.900,p<0.01)、Ca-P(r=0.773,p<0.01)及De-P(r=0.714,p<0.05)含量显著性相关,表明调查海区沉积物中Ads-P具有广泛的来源;与沉积物中TOC(r=0.720,p<0.05)、GSL(r=0.789,p<0.01)、粘土含量(r=0.682,p<0.05)显著性相关,表明有机质的矿化降解和粒度效应是控制沉积物中Ads-P含量的重要因素,反映了沉积物颗粒有机碳含量越高,粒径越小,颗粒比表面积越大,表面吸附能力越强,所以在细颗粒沉积物中,Ads-P含量较高(表2)。此外,Ads-P的含量也与沉积环境有关,在相对还原的环境中Ads-P的含量相对偏高。通常可以把沉积物中硫化物的丰度作为指示沉积物氧化还原状况的重要指标[21],因此沉积物中硫化物与Ads-P之间良好的线性相关关系(r=0.519,p<0.05)可以证实沉积环境对Ads-P的影响(表2)。
沉积物中Fe-P主要是吸附在铁的氧化物和氢氧化物的胶体表面上。由于铁存在氧化还原平衡,容易受到氧化还原电位变化的影响,所以磷的生物地球化学特征就会受到铁的氧化还原特征影响[22]。当三价铁被还原为二价铁时,结合的磷会随着二价铁的溶出而被释放到间隙水,进而在浓度梯度的作用下进入上覆水体,即Fe-P在还原条件下趋向于释放到水体,这表现在Fe-P与沉积物中硫化物含量的相关系数上(r=-0.564,p<0.05)。除此之外,有机碳含量(r=0.680,p<0.05)和沉积物粒度(r=0.715,p<0.05)也是影响Fe-P含量的重要因素(表2),沉积物颗粒有机碳含量越高,其粒径越小,比表面积越大,表面吸附能力就越强,所以有机质降解过程中释放出来的溶解态磷就被铁的(氢)氧化物吸附的越多,Fe-P含量可能越高。Fe-P与沉积物中其它磷形态也均有较好的相关关系(表2),这说明各磷形态与Fe-P可能具有相似的来源。
钙结合态磷是沉积物磷组分中较惰性的一种磷形态,主要包括自生磷灰石及钙结合态磷(Ca-P)和碎屑态磷(De-P)两个部分。其中前者主要是自生成因或生物成因的自生磷灰石,以及与自生碳酸钙共沉淀或外源输入的各种难溶性的磷酸钙矿物,后者主要是来自岩石的风化产物—碎屑氟磷灰石[23]。

表2 表层沉积物不同形态磷与沉积物理化性质之间的相关系数
注:n=5;*表示p<0.05;**表示p<0.01
Ca-P一般可以看作是永久性的磷汇,但当外界环境因素改变时仍会影响Ca-P的含量,如在弱酸性的环境下可以使其产生一定的释放,从而对上覆水体产生影响。相关分析研究表明(表2),大亚湾表层沉积物中Ca-P与其它形态磷具有较好的相关关系(除OP),尤其与IP的相关系数达0.910,这表明Ca-P是IP的主要组成部分,并影响IP的空间分布模式。研究区域内沉积物粒度与Ca-P之间存在显著的正相关关系(r=0.871,p<0.01),反映了细颗粒物质含量越高越有利于Ca-P在沉积物中的累积,这可能要取决于氟磷灰石和碳酸钙自身的物理特征(表2)。研究还发现,沉积物中Ca-P的含量水平与有机质密切相关(r=0.886,p<0.01),由此揭示了Ca-P在沉积物中的分布也与有机质的累积和降解有关(表2)。
大亚湾表层沉积物中De-P的含量与沉积物粒度不存在显著相关性(表2),一般来说,De-P的含量与沉积物的比表面积无关,即沉积物颗粒越细,De-P的含量就越少,这与De-P主要来源于岩石的风化产物-碎屑氟磷灰石有关[24]。
2.3 沉积物中无机形态磷的生物地球化学意义
研究沉积物中磷形态的主要目的是定量生物有效磷,生物有效磷包括沉积物中可释放并参与水体中磷再循环的部分,它与沉积物-水界面磷的交换休戚相关,通过对不同形态磷含量的分析可以确定沉积物中潜在生物有效性磷的上限[25-28]。沉积物中Ads-P是最具生物有效性的磷,当上覆水体中磷酸盐含量较低时,通过沉积物-水界面交换会很容易释放到上覆水体,进而被浮游生物利用;Fe-P具有潜在的生物有效性,在近岸沉积环境处于还原状态时,可使Fe-P发生还原释放磷酸盐;而OP必须矿化降解为无机磷酸盐才更适于生物利用。在近岸环境中,Ca-P和De-P在弱碱性的水环境中活性是很低的,仅在pH骤降时才会溶解出一部分,难以转化为磷酸盐被生物所利用,基本上对沉积物间隙水或上覆水的累积没有任何贡献[29]。因此,大亚湾表层沉积物中的生物有效性磷包括Ads-P、Fe-P和OP[30]。在本次研究中,大亚湾表层沉积物中Ca-P和De-P约占TP的60.73%~69.28%,这些沉积磷不能被生物所利用,而将被埋藏在近岸沉积物中或运移至外海沉积。大亚湾表层沉积物中潜在生物有效性磷的含量为70.87~127.03 mg/kg,仅仅是沉积磷库中的一小部分,平均约占总磷的29.40%。在近岸复杂的物理、化学和生物因素的共同作用下,通过沉积物-水界面过程这些生物有效性磷会发生再生活化,从而在不同程度上会促进藻类生长、影响水体的富营养化状态和初级生产力。
3 结 论
大亚湾表层沉积物中的磷以无机形态磷为主,平均达85.11%,而无机形态磷又以De-P和Ca-P为主。在空间分布上,各形态磷主要受陆源输入因素的控制。
相关分析表明,Ads-P、Fe-P、Ca-P、De-P具有相似的物质来源;GSL是控制Ads-P、Ca-P、De-P的重要因素;沉积环境是影响Fe-P含量的重要因素。
Ads-P、Fe-P、OP是大亚湾表层沉积物中潜在的生物有效性磷,平均约占总磷的29.40%,是沉积磷中的活性磷;De-P、Ca-P是沉积物中的惰性磷,基本不参与磷的生物地球化学循环。
参考文献:
[1] DUAN Y,SONG J M,ZHANG H.Carbon isotopic studies of individual lipids in organisms from the Nansha sea area[J]. Science in China:Series D, 2004,47(7): 593-598.
[2] 宋金明,李学刚,邵君波,等.南黄海沉积物中氮、磷的生物地球化学行为[J].海洋与湖沼,2006,37(4):370-376.
[3] CIBLIN A E.Benthic metabolism and nutrient cycling in Boston Harbon[J].Massachusetts Estuaries,1997,20(2):346-364.
[4] ZABEL M,DAHMKE A,SCHULZ H D.Reginal distribution of diffusive phosphate and silicate fluxes through the sediment-water interface: The eastern south Atlantic[J].Deep Sea Research,1998,1(45):277-300.
[5] HARTER R D.Adsorption of phosphorus by lake sediments[J].Soil Sci Am Proc,1968,32:514-518.
[6] 吴芳,郭卫东,郑佩如,等.三都澳养殖海域沉积物中P的形态分布特征[J].海洋环境科学,2005,24(4):24-27.
[7] 徐恭昭.大亚湾环境与资源[M].合肥:安徽科技出版社,1989,5-6.
[8] 丘耀文.大亚湾营养物质变异特征[J].海洋学报,2001,23(1):85-93.
[9] 孙丽华,王肇鼎,彭云辉.大亚湾海域海水中各种形态磷的研究[J].海洋环境科学,2005,24(4):28-32.
[10] 丘耀文,王肇鼎,朱良生.大亚湾海域营养盐与叶绿素含量的变化趋势及其对生态环境的影响[J].台湾海峡,2005,24(2):131-139.
[11] 何桐,谢健,方宏达,等.大亚湾海域春季营养现状分析与评价[J].海洋环境科学,2008,27(3):220-223.
[12] 丘耀文,王肇鼎,高红莲,等.大亚湾养殖水域沉积物-海水界面营养盐扩散通量[J].热带海洋,1999,18(3):83-90.
[13] 李占东,林 钦,黄洪辉.大鹏澳网箱养殖海域磷酸盐在沉积物-海水界面交换速率的研究[J].南方水产,2006,2(6):25-30.
[14] 何清溪,张穗,方正信,等.大亚湾沉积物中氮和磷的地球化学形态分配特征[J].热带海洋学报,1992,11(2):38-45.
[15] RUTTENBERG K C.Development of a Sequential Extraction Method for Different Forms of Phosphorus in Marine Sediments[J].Limnology and Oceanography,1992,37(7):1460-1482.
[16] 李学刚,宋金明,牛丽凤,等.近海沉积物中氮磷的同时测定及其在胶州湾沉积物中的应用[J].岩矿测试,2007,26(2):87-92.
[17] 岳维忠,黄小平,孙翠慈,等.珠江口表层沉积物中氮、磷的形态分布特征及污染评价[J].海洋与湖沼,2007,38(2):111-117.
[18] 卢博,张福生,黄韶健,等.大亚湾表层沉积物性质及其对海水养殖的影响[J].台湾海峡,2002,21(4):489-495.
[19] 姜双城,郑爱榕,林培梅.北部湾南部沉积物中磷的形态特征及环境意义[J].厦门大学学报,2008,47(3):438-444.
[20] 戴纪翠,宋金明,李学刚,等.胶州湾沉积物中的磷及其环境指示意义[J].环境科学,2006,27 (10):1953-1962.
[21] 王文强,韦献革,温琰茂.哑铃湾网箱养殖对表层沉积物的污染[J].热带海洋学报,2006,25 (1):56-60.
[22] 岳维忠,黄小平.近海沉积物中氮磷的生物地球化学研究进展[J].台湾海峡,2003,22(3):407-414.
[23] RUTTENBERG K C,BERNER R.Authigenic apatite formation and burial in sediments from non-upwelling,continental margin environments[J].Geochimica et Cosmochimica Acta,1993,57: 991-1007.
[24] 李敏,韦鹤平,王光谦,等.长江口、杭州湾水域沉积物中磷的化学形态分布特征[J].海洋学报,2004,26(2):125-131.
[25] 蒋增杰,方建光,张继红,等.桑沟湾沉积物中磷的赋存形态及生物有效性[J].环境科学,2007,28(12):2783-2788.
[26] ANDRIEUX F,AMIONT A.A two year survey of phosphorus speciation in the sediments of the Bay off Seine(France)[J].Continental Shelf Research,1997,17(10):1229-1245.
[27] LIU S M,ZHANG J,LI D J.Phosphorus cycling in sediments of the Bohai and Yellow seas[J]. Estuarine,Coastal and Shelf Science,2004,59(2):209-218.
[28] 戴纪翠,宋金明,李学刚,等.胶州湾不同形态磷的沉积记录及生物可利用性研究[J].环境科学,2007,28(5):929-936.
[29] JIANG Z J,FANG J G,ZHANG J H,et al.Forms and Bioavailability of Phosphorus in Surface Sediments from Sungo Bay[J].Environmental Science,2007,28(12):2783-2788.
[30] 侯立军,陆健健,刘敏,等.长江口沙洲表层沉积物磷的赋存形态及生物有效性[J].环境科学学报,2006,26(3):488-494.
