重金属在水体中迁移转化过程分析
2010-04-25李莉,张卫,白娟,宋炜
李 莉,张 卫,白 娟,宋 炜
(山东省水利勘测设计院,山东 济南 250013)
重金属污染物进入水体后由于水体中悬浮物的吸附作用,大部分从水相转移至悬浮物中随之迁移,当悬浮物负荷量超过其搬用能力时就逐步沉降下来,蓄积在沉积物中。水环境条件等因素改变时,重金属又可能再次释放,重新进入水体中。由此可见,重金属在水体中的迁移转化是一个复杂的过程,包括了水体中的各种物理、化学及生物反应,并且其中有些过程是可逆的,所以在研究重金属在水体中的迁移转化规律时,必须综合考虑各过程以及主要影响因素。由于迁移转化规律复杂,在水环境条件的影响下,不同的重金属污染物之间也会反映出明显的差异,因此本文主要是分析重金属污染物在水体中的迁移转化规律的共性。
在重金属迁移转化中有两个环节是十分重要的:①重金属被吸附,这是重金属污染物沉降的前提条件。重金属如何被吸附,吸附量和吸附速率受哪些因素的影响,都直接关系到重金属能否很快的迁移到沉积物中;②重金属的释放。重金属从悬浮物或沉积物中重新释放,造成二次污染,对其释放规律和影响因素的研究十分必要。
1 重金属的吸附过程
1.1 影响重金属吸附的主要因素
进入天然水体中的重金属污染物被水体中的悬浮沉积物吸附,它们顺水迁移或经絮凝沉降到底部沉积物中,这是重金属污染物由液相转入固相的重要途径,也是水相浓度降低的主要原因。因此,重金属的吸附过程是其迁移转化过程中的重要环节,对水体的自净、污染效应以及控制措施等都有直接的影响。影响重金属吸附的水力环境因素是研究所关注的重点,经分析主要有以下几个方面:
1.1.1 悬浮物
悬浮物是水体污染物的主要载体,悬浮物中多含有较强吸附能力的活性物质,主要是粘土矿物、铁锰水和氧化物、有机物以及碳酸盐等,它们的种类和特性决定着悬浮沉积物的吸附性能。因此在对悬浮沉积物的整体吸附性能进行研究时,也要对其中各组分进行单独吸附能力分析,考察它们对于总体吸附的贡献。除了悬浮物的吸附特性外,悬浮物浓度和粒径大小也是影响重金属悬浮的重要因素。研究表明,在重金属污染物浓度固定时,单位吸附量随着悬浮物浓度增加而减小,并且随着粒度的增大悬浮物对污染物的吸附量减少[1]。
悬浮物在污染物的输送以及最终归宿方面起到很重要的作用,对于重金属污染物亦是如此。目前主要通过现场采样调查和实验分析相结合的方式,分析悬浮物的表面特性等对重金属的吸附以及迁移能力的影响,杨晓兰[2]、邬建中[3]等在这方面都作过相关研究。
1.1.2 泥沙性质
在多泥沙河流中,泥沙是沉降物的主体,悬浮物中以细颗粒泥沙为主,而沉积物中则以粗颗粒泥沙为主,泥沙成为了多泥沙河流中重金属污染物的主要归宿[4]。张书农等最先倡导 “运用泥沙分析河流重金属污染”。可见,泥沙对于多泥沙河流中重金属污染问题研究的重要性。经研究发现泥沙浓度和泥沙性质是多泥沙河流中影响重金属吸附的最主要因素。
(1)泥沙浓度。研究表明,泥沙浓度与单位泥沙的吸附量呈负相关,这与悬浮物浓度对污染物吸附的影响有着相似性,即泥沙浓度减少,单位泥沙的吸附量增加,但吸附总量总是随着含沙量的增加而不断增加的。这是因为泥沙含量小时,泥沙表面可充分与水溶液接触,可有效吸附重金属;而当泥沙含量逐渐增大时,由于泥沙的相互粘结使得与水溶液直接接触的表面吸附点位以及水相重金属浓度逐渐减小,单位泥沙的吸附量受到相应影响。
(2)泥沙粒径。泥沙吸附与其比表面积(表面积/体积)也有一定关系,若将泥沙近似认为是球体,则其比表面积与粒径成反比,泥沙越细,比表面积越大,具有越多的空白吸附点位,所以吸附作用就越强。实验研究也证明,细粒径泥沙吸附能力强,而粒径大的泥沙吸附能力较弱,尤其在重金属浓度较高时,表现更为明显[5]。
泥沙的吸附作用除了与上述两种因素有关外,还与泥沙颗粒所含的活性成分有关,泥沙的活性成分通常是指粘土矿物、铁、锰、铝水合氧化物和碳酸盐等。一般颗粒越细,所含活性成分越多,这与泥沙粒径的影响是相同的。
1.1.3 沉积物
沉积物对重金属吸附的影响类似于悬浮物。沉积物中的有机质、矿物等都对很多重金属有很强的吸附能力,其组分和含量的不同影响其对重金属的吸附能力,并且也具有细微颗粒吸附重金属量大的特点。
1.1.4 温度和pH值
随着温度的升高,重金属的吸附速率增大。金相灿在研究黄河中游悬浮物对重金属吸附和解吸中就得到类似结论:随着反应温度升高Cu被沉积物吸附的速率逐渐升高。
由于pH值变化会制约重金属的溶解度等很多性质,而且还会影响悬浮沉积物的表面吸附特性和各种吸附反应,所以水体pH值的变化直接影响吸附速率的变化,通常pH值升高吸附速率增大,解吸速率减少。吸附量也不是随着pH值的升高无限制的增加,存在一个临界pH值,即在此pH值下吸附量最大[6]。
1.1.5 离子强度
沉积物中有大量的阳离子,如Ca2+、Mg2+、Na+和K+等,它们都会对吸附产生影响,且影响程度不一。Handen等研究Chapala湖沉积物的吸附时发现对Cd的吸附主要依赖于电解质的类型和浓度,而Pb受电解质的影响较小,当浓度增加时,Pb和沉积物表面吸附反应应几乎不可逆[7]。
1.2 重金属吸附模式分析
天然水体中,上述几种因素分别对重金属吸附产生影响,当要综合分析它们对重金属吸附过程的影响时,人们发现可用三种等温吸附模式,即Henry型、Langmuir型和Freundich型,来描述重金属的吸附过程,三种吸附模式分别有不同的适用条件[8]。吸附等温式和吸附动力学方程是三种模式的数学表达形式,其中,吸附等温式是在温度固定条件下表达重金属平衡吸附量和水相平衡浓度之间关系的数学式,根据这种关系绘制的曲线称为吸附等温线,通过该曲线可以研究两者之间的相关关系。吸附动力学方程描述的重金属吸附量随时间的变化过程,主要通过分析吸附和解吸速率来实现。
1.2.1 Henry型
适合于研究重金属污染很低时的吸附情况。

式中:k1为吸附速率系数;k2为解吸速率系数;k3为吸附——解吸系数常数 (=k1/k2);N∞为平衡吸附量;C∞为水相平衡浓度。
由式(1)可见和水相重金属浓度C成正比,与吸附量N成反比;式(2)表明,吸附平衡时,平衡吸附量和水相平衡浓度成正比例。
1.2.2 Freundich型
该模式限于中等浓度的情况。

式中kb和 n为常数,没有明确的物理意义,k1、k2、N∞、C∞同上。
1.2.3 Langmuir型
该模式适合于研究高浓度的重金属吸附情况。
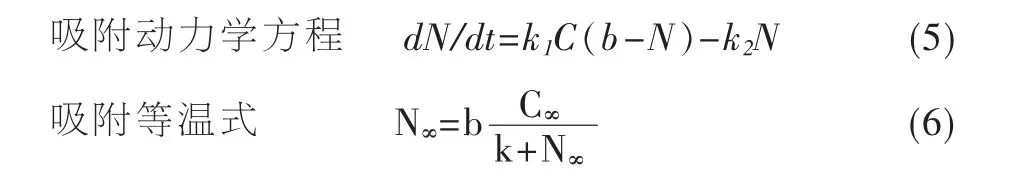
式中 N、C、N∞、C∞意义同上;b 为吸附达到饱和时的最大极限吸附量;k值为吸附系数,相当于吸附量1/2时的水相平衡浓度(=k2/k1)。式(5)表明吸附速率和水相浓度C及剩余吸附能力(b-N)的乘积成正比,与吸附量N成反比。
根据不同的使用条件选择相应的吸附模式,就可以求解出吸附速率和解吸速率系数,并通过改变实验条件分析该数受哪些因素影响,建立它们之间定量或定性关系,从而达到研究重金属吸附的目的。崔慧敏在研究拒马河悬浮沉积物随重金属的吸附——解吸规律时,就用Freundich型吸附等温式求解吸附和解吸系数,并根据影响因素建立了经验公式[9]。黄岁樑等也选用Freundich型和Langmuir型吸附模式研究泥沙对重金属的吸附作用[8]。
除了上述三种吸附模式以外,Stumn等提出的表面络合模式也是近年来用于描述水环境界面上吸附过程的主流理论之一[10]。文湘华等采用该模式对乐安江沉积物的表面特性以及对重金属的吸附特性进行分析,这种模式已建立了相应的图解、参数估值法和计算程序软件[11]。
2 水体中重金属的释放过程
2.1 重金属释放原因
累积于悬浮物或沉积物中的重金属还会被重金属释放出来,这对水生生态系统和饮用水的供给都是十分危险的。水体中的重金属被释放主要由4种化学变化引起:[12]
2.1.1 盐度的变化
在盐度大的水中,由于阳离子竞争加强可被沉积物吸附的金属离子置换出来,这在河海混合带即河口环境中尤为突出。目前人们对河口重金属解吸的研究还主要是针对几种代表性的重金属元素,依据环境特点分析解吸的顺序、速率以及影响因素等。
2.1.2 氧化还原反应条件的变化
在氧化电位下降时,强还原性沉积物中的铁氧化物部分或全部溶解,被其吸附或沉淀下来的重金属离子也同时被释放出来。
2.1.3 pH值的变化
水体pH值降低可使碳酸盐和氢氧化物溶解,H+的竞争吸附作用可增加重金属离子的解吸量。例如从废矿石中渗出的水pH值很低,这种矿石的长期堆放就会促使附近水体中重金属的释放,造成水相重金属浓度的增加。
2.1.4 天然或人工合成的强络合剂的使用
这类络合剂能和重金属形成可溶性络合物,有时这种络合物稳定性较好,可以溶解态存在,这就使重金属解吸出来。
此外,微生物的活动也会引起重金属的释放,主要通过络合金属离子、改变环境条件以及氧化还原等方式促使重金属的释放。
除了上述因素影响之外,重金属释放还与颗粒粒径、颗粒表面特性以及水流紊动强度等因素有关。一般粒径大解吸能力强,水流紊动强度可通过影响水流挟沙力来影响重金属的释放。
2.2 释放过程研究方法的讨论
重金属的释放过程从表面形式上来看似乎是金属吸附过程的逆过程,其实两者之间存在较大的区别:①重金属的解吸速率与吸附速率系数往往相差几个至几十个数量级,两者几乎没有可比性;②由于重金属的吸附速率快,吸附平衡在较短时间内即可达到,而重金属的解吸速率很小,达到释放平衡所需时间很长;③在释放过程中重金属水相浓度并不是单调地增加直至平衡,而是经历了由低到高,再下降直至平衡的过程,这不同于一般的解吸过程。主要是因为在重金属释放到一定程度时又与其它溶出物质发生物理化学变化,从而使水相重金属浓度又开始降低直至平衡,所以浓度值存在峰值。
对重金属在水体中释放规律的研究主要有两种方法。一种方法是以重金属吸附动力学为基础,把重金属释放看作是吸附的逆过程。文献[13]中在研究释放动力学方程中的系数时就用Freundich型吸附模式中的解吸系数代替,正是从这种角度来研究重金属的解吸过程。另一种方法则是以重金属释放的试验为基础,研究重金属释放的动力学过程。
选择第一种方法研究重金属释放问题,需要考虑的是用重金属吸附动力学模型来描述重金属的释放动力学过程是否合理。通过对吸附和释放过程区别的分析,可以看出释放过程并不能完全等同于吸附过程的逆过程,通过以吸附为主要研究对象的试验来反映释放规律并不是很准确。若从第二种方法出发,释放过程十分缓慢,实验室的水流实验受到限制,也使得研究十分困难。目前对重金属释放过程的研究还处于发展中,释放动力学模型理论依据不足,各种影响因素的研究中定量描述少,多为定性描述。而且大部分成果都是室内试验得出来的,如何将其更好的应用到复杂的天然水体中有待进一步讨论。
[1]陈静生,周家义.中国水环境重金属研究[M].中国环境科学出版社,1992.
[2]杨晓兰.长江口悬浮颗粒物的表面特性与重金属的沉降[J].环境污染与防治,1999,21(3).
[3]邬建中,黄爱珠.浈水水体的重金属迁移与吸附特性[J].人民珠江,1996,2.
[4]张书农等.水环境污染规律研究 [J].河海大学科技情报,1990,3.
[5]Tessier A,Campbell P G C and Bisson M.Sequential extraction procedure for the speciation of particulate trace metals[J].Analytical Chemistry,1979,51(7).
[6]王晓蓉.金沙江重金属在颗粒物中的分布及基本特征[J].环境化学,1983,2(1).
[7]Hansen A M,Maya P.Adsorption-desorption behaviors of Pb and Cd in Lake Chapala,Mexico [J].Enviormental Intemational,1997,23(24).
[8]黄岁樑,万兆惠,王香兰.泥沙吸附重金属污染物室内静态试验研究[J].水科学进展,1994,5(4).
[9]崔慧敏.拒马河悬浮沉积物对重金属的吸附一解析研究[J].水资源保护,2000,59(1).
[10]Stumn W,Huang CP,Jenkins S R.Specific chemical interaction affecting the stability of dispersed systems[J].Croatica..Chim.Acta.,1970,42.
[11]文湘华,杜青等.乐安江沉积物对重金属的吸附模式研究[J].环境科学学报,1996,16(1).
[12]周密,王华东,张义生.环境容量[M].长春:东北师范大学出版社,1987.
[13]金相灿等.湘江重金属迁移转化模型研究[J].中国环境科学,1987,7(6).
