均三氮苯类除草剂的定量构效关系研究
2010-01-25刘翠,金飙,金俏
刘 翠, 金 飙, 金 俏
(1.沈阳化工大学环境与生物工程学院,辽宁沈阳110142; 2.北京石油化工学院化学工程学院,北京102600)
均三氮苯类除草剂在国内外应用广泛,除草效果好,杀草谱广,成本低廉,但其在土壤中的残留期较长,并易对水体造成污染,对生物和人类具有蓄积毒性,因此,该类除草剂所带来的环境问题也日益受到人们的关注[1-7].目前,对于除草剂类物质的定量结构-活性相关(Quantitative Structure-Activity Relationship,QSAR)研究发展迅速,而量子化学参数由于计算简便、物理化学意义明确,在建立QSAR模型中得到广泛关注和应用[8-13].本研究运用量子化学参数法建立均三氮苯类除草剂的QSAR模型,在最稳定的分子构型下得到该类物质的除草活性与其结构之间的量变关系,为预测相似结构化合物的除草活性提供依据.
1 研究方法
研究对象选用应用十分广泛的10种均三氮苯类除草剂:西玛津、莠去津、扑灭津、草达津、莠去通、西玛通、西草净、敌草净、莠灭净、扑草净.研究采用均三氮苯类除草剂对杂草的抑制中浓度的负对数 PI50值作为该类化合物的除草活性数据,PI50值引自文献[14].
研究方法采用量子化学方法.量子化学参数比传统的经验参数在描述化合物结构上要更加全面,物理意义更加明确,利用量化参数研究化合物的生物活性以及预测化学品的理化性质已获得很大成功.所以,将量子化学方法引入QSAR研究已成为一个大方向[15-20].研究采用 HF方法和密度泛函理论中的B3LYP方法,对化合物的分子结构及化学性质进行系统的理论研究,通过量子化学计算,可全面获得有关分子的电子结构和几何结构的信息,如分子轨道能量、偶极矩、原子电荷密度等,并利用计算获得的量子化学参数建立均三氮苯类除草剂的定量构效关系模型.
运用Chem3D、ChemDraw等化学绘图及模拟软件进行均三氮苯类化合物的分子设计和构型设计;在B3L YP/6-31G*和 HF/6-31G*水平下,对化合物进行几何构型优化,使用 Gaussian03软件计算得出化合物的偶极矩、电子亲和势、EHOMO和 ELUMO等量化参数,并对 PI50值与各量化参数进行相关性分析;应用SPSS 11.5统计程序,在95%置信区间内,采用逐步回归分析方法,建立均三氮苯类化合物的除草活性与其结构之间的QSAR相关模型,为预测该类化合物的除草活性以及相似结构化合物的除草活性提供理论依据.
2 结果与讨论
2.1 量子化学计算结果
在B3L YP/6-31G*和 HF/6-31G*水平下,计算得出所选取的10种均三氮苯类化合物的分子总能量 E、零点振动能 EZP、最低振动频率 fL、最高占据轨道能量 EHOMO、最低空轨道能量ELOMO、最高占据轨道和最低空轨道之间的能量间隙ΔE、偶极矩μ、偶极矩的平方μ2、苯环上取代基氮原子所带的电荷数Q1、Q2等量子化学参数.计算结果见表1,量化参数见表2和表3.

表1 10种均三氮苯类化合物总能量 E(kJ/mol)、零点振动能 EZP(kJ/mol)、频率(cm-1)(红外振动强度)Table 1 The total energy,zero-point energy,the lowest frequency(infrared vibration strength)of herbicides

表2 B3L YP/6-31G*水平下均三氮苯类化合物的量子化学参数Table 2 Quantum chemistry and activities parameters of herbicides at the level of B3L YP/6-31G*
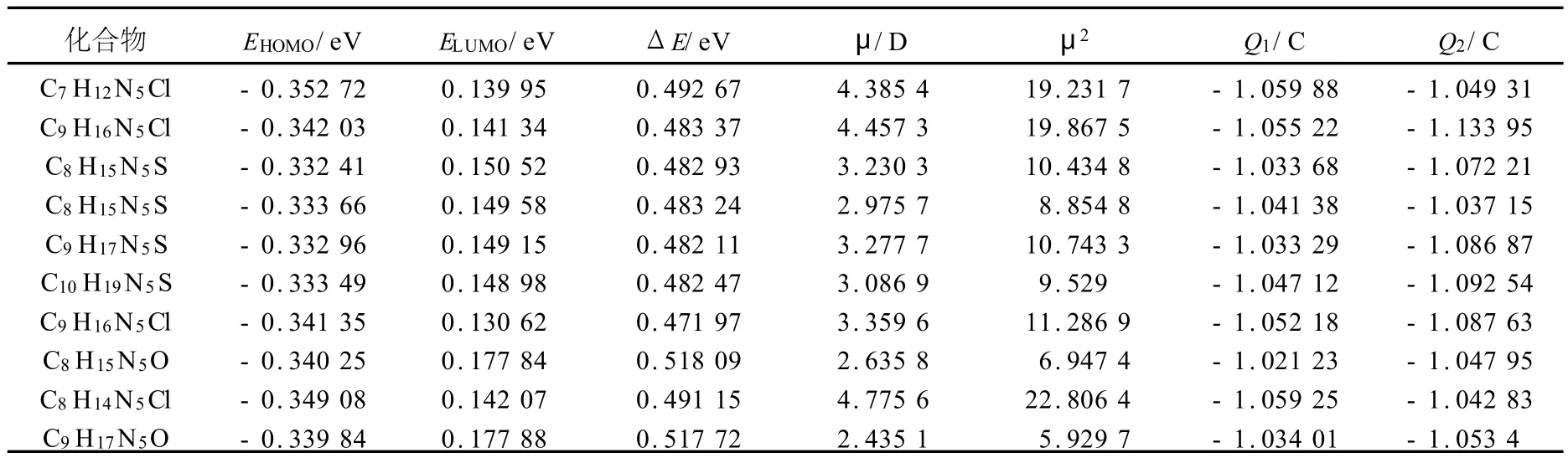
表3 HF/6-31G*水平下均三氮苯类化合物的量子化学参数Table 3 Quantum chemistry and activities parameters of herbicides at the level of HF/6-31G*
2.2 参数选择和相关性分析
应用SPSS 11.5软件对PI50值与各量化参数间进行相关性分析,见表4和表5.

表4 B3L YP/6-31G*水平下均三氮苯类化合物 PI50的相关系数Table 4 Coefficients of independent variables at the level of B3L YP/6-31G*
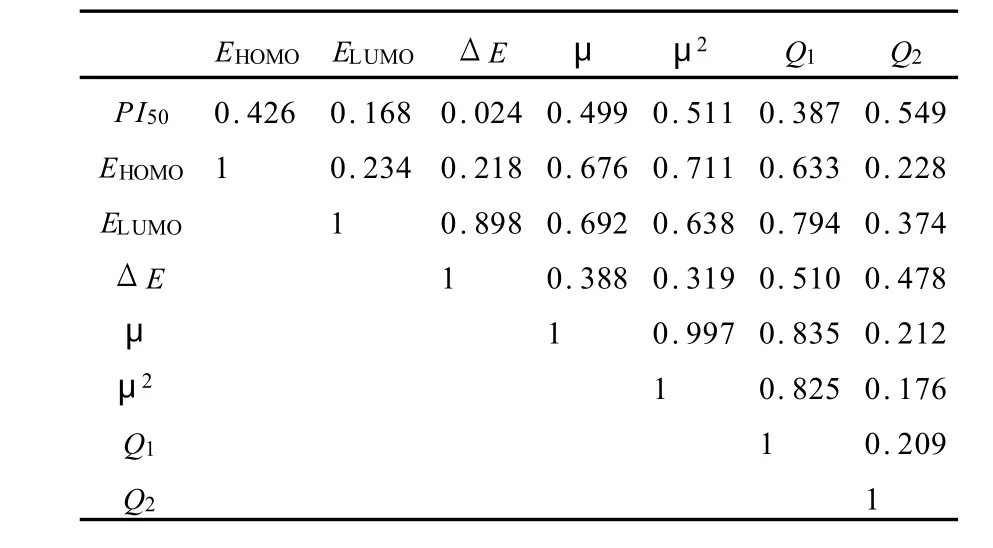
表5 HF/6-31G*水平下均三氮苯类化合物 PI50的相关系数Table 5 Coefficients of independent variables at the level of HF/6-31G*
正数为正相关,负数为负相关.在回归中将体现相关性,对于大于0.5的为强相关,对回归方程为重要变量;对于小于0.5的或为负的均为弱相关或不相关,在回归中将不考虑他们对回归方程的影响.
在相关系数表中,可以明显地看出每个参数之间的相关性.对均三氮苯类化合物预测的决定因素做出了比较.对决定物质除草活性的主要因素也能够得到初步的体现,更具体的将在回归方程中体现.
由表4和表5可看出:两表中μ与μ2的相关系数均高达0.977,根据统计学原理,两变量间相关系数超过0.98,则认为其存在共线性现象,不能同时出现在同一方程中,必须删去其一.
2.3 建立QSAR方程
运用SPSS软件采用多元逐步回归的方法对数据进行处理,最后得到如下回归方程:
B3L YP回归方程: HF回归方程:
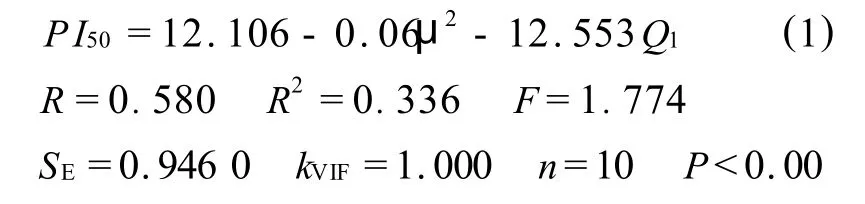

其中,R是相关系数,R2表示决定系数,F是检验值(用来检验回归拟和程度的好坏),SE是标准误差,kVIF是变异膨胀系数,n是样本量, P表示显著性水平.
由回归方程可以看出,均三氮苯类化合物的除草活性(即其对杂草的抑制中浓度的负对数PI50)与化合物分子偶极距的平方μ2和苯环上取代基氮原子所带的电荷数Q1呈负相关关系. μ2和 Q1越大,该类化合物对杂草的抑制作用PI50就越小,除草活性则越小.
极性是分子重要的理化参数,并且偶极矩反映了整个分子的极性,在一定程度上反映了化合物和生物受体分子之间相互作用的大小.通过回归方程表明,均三氮苯类除草剂的结构参数——偶极矩对于该类化合物除草活性的影响是非常重要的.
2.4 QSAR模型的检验
对B3L YP和 HF两种方法 PI50的实验值与计算值进行残差分析,见表6和表7.
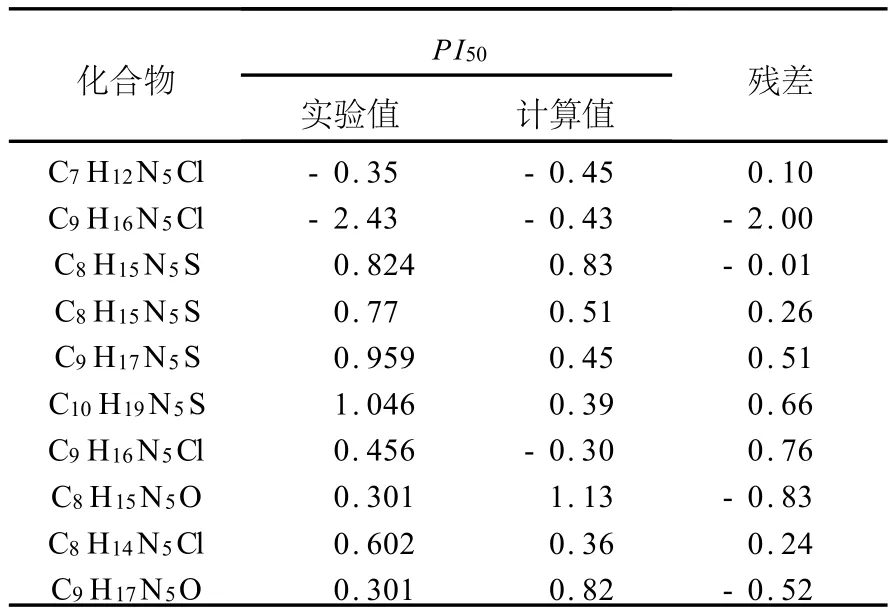
表6 在B3L YP/6-31G*水平下根据方程(1)得出的 PI50计算值与实验值的残差Table 6 The calculation and residuals at the level of B3L YP/6-31G*

表7 在HF/6-31G*水平下根据方程(2)得出的PI50计算值与实验值的残差Table 7 The calculation and residuals at the level of HF/6-31G*
由表6、表7可以看出:两种方法下,10种均三氮苯类化合物的除草活性 PI50的计算值与实验测定值基本符合.
3 结 论
分别采用B3L YP和 HF两种量子化学方法,使用6-31G*基组计算了10种均三氮苯类除草剂的多个量子化学参数,建立该类化合物的除草活性与其结构间的QSAR模型.结果表明:均三氮苯类化合物对杂草的抑制中浓度的负对数PI50与其结构参数之间存在着一定的线性相关性.其除草活性 PI50与化合物分子偶极距的平方μ2和苯环上取代基氮原子所带的电荷数Q1呈负相关关系.μ2和 Q1越大,PI50则越小,即该类化合物的除草活性越小,这说明分子偶极距和苯环上取代基氮原子所带的电荷数是影响均三氮苯类除草剂除草活性的重要因素.
[1] 刘长令.世界农药大全——除草剂卷[M].北京:化学工业出版社,2002:932-965.
[2] 朱永春,张小英,高宇.苯酚衍生物式电位的QSAR研究[J].计算机与应用化学,2005,9(22): 771-774.
[3] 张玉聚,张德胜,张俊涛,等.三嗪类除草剂的创制经纬[J].农药,2003,42(4):42-44.
[4] 王麦华,王成业,张海申,等.降解均三嗪类除草剂的优势菌的特性研究[J].农业与技术,2005,25 (1):120-122.
[5] Sukekawa M,Nakayama A.Molecular Shape Similarity Between Cyclic Imides and Protoporphyrinogen IX[J].Pestic Sci.,1999,55(3):345-347.
[6] Yukio N,Nobuhide W,Fumitaka Y,et al.Quantitative Structure-activity Relationships ofDimethoxypyrimidinyl(thio)salicylic Ac-idat[J].Peatic Sci.,1998,52(4):343.
[7] 姜晖霞.均三氮苯类除草剂的定量构效关系研究[D].湖南:湖南农业大学,2005:45-48.
[8] 于瑞莲,胡恭任.不同p H值下对发光菌的毒性及QSAR研究[J].环境科学与技术,2005,4(28):20 -22.
[9] Vera K,Karel P.Combination of Molecular Modeling and QSAR Analysis[J].Inter J Parm,2004, 21(2):224-226.
[10]Prashanth Athri,Tanja Wenzler,Patricia Ruiz,et al.3D QSAR on a Library of Heterocyclic Diamidine Derivatives with Antiparasitic Activity[J]. Bioorganic&Medicinal Chemistry,2006,14(9): 3144-3145.
[11]YAN X F,XIAO H M.QSAR Study of Nitrobenzenes’Toxicity to Tetrahymena Pyriformis Using Semi-empirical Quantum Chemical Methods[J]. Struct.Chem.,2007,26(1):7-14.
[12]星炯浩,张运陶.卤代酚对水生梨形四膜虫急锐毒性的QSAR研究[J].计算机与应用化学,2007,24 (1):87-90.
[13]崔秀君,王志欣,袁星,等.支持向量机用于酚类化合物毒性的QSAR研究[J].计算机与应用化学, 2008,25(3):298-302.
[14]赵善欢.植物化学保护[M].北京:中国农业出版社,1996:318-319.
[15]Cronin M T D,Schultz T W.Structure-toxicity Relationships for PhenolsTo Tetrahymena Pyriformis [J].Chemosphere,1996,32(8):1453-1468.
[16]沈斌,张哗,裴剑锋,等.家蝇GABA受体抑制剂的比较分子相似性指数分析模型研究[J].计算机与应用化学,2004,21(2):224-226.
[17]毛明现,余训民,胡立嵩,等.氯代苯及酚类化合物对生物毒性的定量研究[J].武汉工程大学学报, 2008,30(3):60-64.
[18]Hansch C.Structure-activity Relationships[M]. New York:Permon Elmsford,1973:113-115.
[19]杨光富,杨华铮.啼陡(硫)醚类除草剂的非线性QSAR研究[J].华中师范大学学报,2001,35(1): 40-44.
[20]戴玄吏,王晓栋,黄宏,等.应用分子全息QSAR技术预测硝基芳烃的遗传毒性[J].环境科学学报, 2003,23(5):674-678.
